ベンチャーが先導する再生医療、臓器移植の代替も視野に応用研究が進む
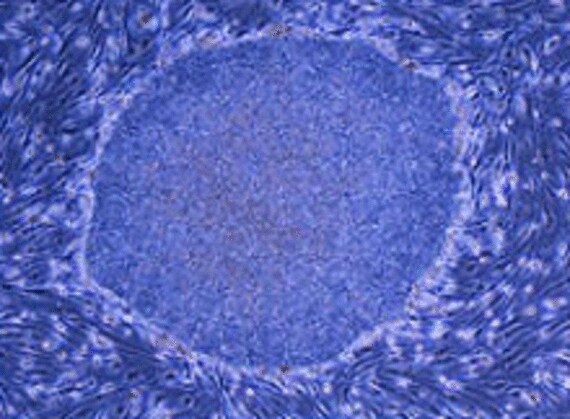 iPS細胞の研究については、世界中でデッドヒートが続いている。山中教授のチームはiPS細胞を人体に導入しても細胞が腫瘍(がん)化しないための方法を研究中だ。
iPS細胞の研究については、世界中でデッドヒートが続いている。山中教授のチームはiPS細胞を人体に導入しても細胞が腫瘍(がん)化しないための方法を研究中だ。
iPS細胞はどんな細胞にも分化できるが、せっかくある臓器を作製しても、意図しない別の細胞に分化して増殖する可能性がある。iPS細胞樹立に用いた4因子のうち「c−Myc」は本来、がん遺伝子だった。そこで山中チームはc−Mycを除く3因子でiPS細胞を作製しマウスに移植したところ、300日経っても腫瘍化を抑制できた。
また、人種、性別、年齢の異なる25人の被験者全員からiPS細胞を作ることにも成功。81歳の女性から作ったiPS細胞では、細胞分裂のたびに短くなる染色体末端の「テロメア」と呼ばれる部分が、6歳女児から作ったiPS細胞と同じ長さに戻っていた。老化した高齢者から作ったiPS細胞でも、若々しい臓器や器官に分化しうることがわかった。
一方、米国では08年8月、ハーバード大学のジョージ・デイリー准教授らの研究チームが、パーキンソン病や筋ジストロフィーなど10種類の患者の体細胞からiPS細胞の作製に成功。今年3月には、英国エディンバラ大学などのチームが、iPS細胞を作るための特定4遺伝子を体細胞内に運ぶ手段として、発がんリスクのあるウイルスでなく、プラスミドと呼ばれる環状DNAや、タンパク質を小さくしたペプチドを用いることに成功したと相次ぎ発表。iPS細胞の安全性を高めるための基礎研究が繰り広げられている。
これに対して、もっと治療現場に近い臨床研究者は、iPS細胞やES細胞よりも最終目標の臓器・器官に近い「体性幹細胞」を研究のターゲットにしてきた。
体性幹細胞は骨、神経、臓器など体の各部位に存在する。「幹」と名付けられているのは、最終的な形態に「枝分かれ」する前段階にあるからだ。とはいえ、iPS細胞やES細胞に比べれば実際の臓器や器官に近いところまで分化しているため、がん化する可能性は低い。






























