11歳小児がん患者が直面「ドラッグロス」の絶望 海外製薬ベンチャーが日本での臨床開発を除外
厚生労働省によれば、23年3月時点で欧米にて承認された薬のうち、日本では143の薬が未承認だった。しかもそのうち約6割は、日本での承認に向けた開発すら行われていなかった。
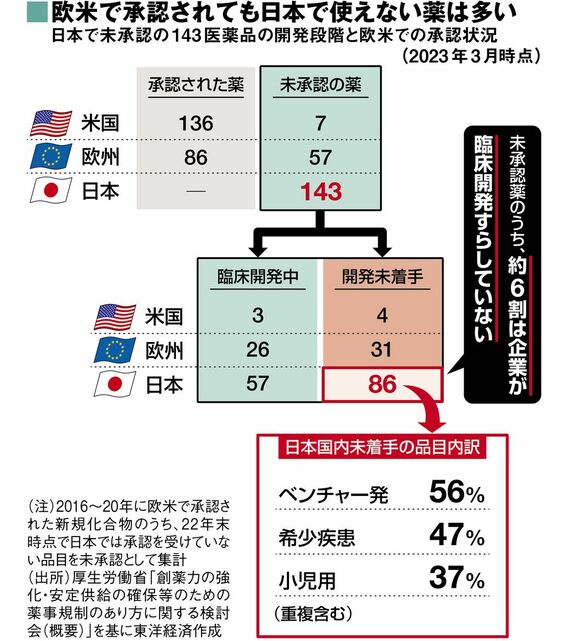
新たな薬を生み出す主体はベンチャー企業に
新たな薬を生み出す主体は今、大手製薬企業から、小規模なベンチャー企業に移っている。大門さんが知った「次の薬候補」も、売上高ゼロの米ベンチャー「デイ・ワン・バイオファーマシューティカルズ」が開発したものだ(7月にフランスの製薬企業イプセンが米国以外での商業権を獲得)。
ベンチャーにとっては、売り上げが小さな希少疾患薬でも十分なリターンとなる。米国はベンチャーへの投資資金が潤沢で、研究開発を迅速に進められる。こうした理由から、米国では希少疾患などのニッチな領域で開発に果敢に取り組む企業が増えてきた。
問題は、これらの企業が日本向けに開発を行うとは限らないということだ。その理由の1つが、日本の薬事制度だ。例えば日本では、日本人が治験に参加していることが承認条件となる。


































無料会員登録はこちら
ログインはこちら